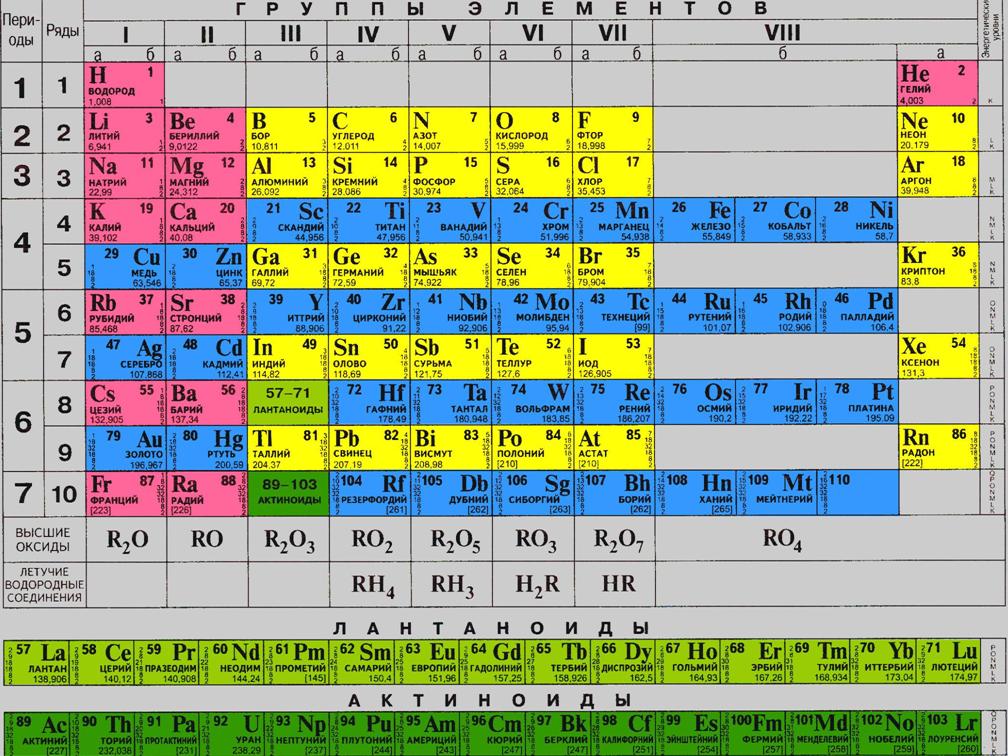
Периодический закон Менделеева – одна из фундаментальных основ современной химии. Этот закон установлен российским химиком Дмитрием Менделеевым в 1869 году и является ключевым для классификации и систематизации элементов.
Основная идея закона заключается в том, что химические элементы можно упорядочить по возрастающему атомному номеру (количеству протонов в ядре атома), так, чтобы элементы с подобными химическими свойствами находились в одной вертикальной группе. Это позволяет установить закономерности в химическом поведении элементов и предсказывать свойства недостающих веществ.
Периодический закон Менделеева был важным шагом в развитии химии, так как он существенно упростил и систематизировал знания о химических элементах. Он стал основой для создания периодической системы, которая является удобным и эффективным инструментом для изучения свойств химических веществ и проведения реакций.
В периодической системе элементы расположены в порядке возрастания их атомного номера и группируются в горизонтальные ряды, называемые периодами, и вертикальные столбцы, называемые группами. Каждый элемент имеет свой символ (обозначение), а также атомный номер и атомную массу. Кроме того, в периодической системе указываются основные химические свойства элементов и их важные физические показатели.
Знание периодической системы позволяет понять и предсказать множество химических реакций и свойств веществ. Оно является основой для понимания состава веществ, разработки новых материалов, анализа веществ и многих других областей химии. Без периодической системы и периодического закона Менделеева современная химия была бы невообразима.
Статья о периодическом законе Менделеева и периодической системе
Первоначально Менделеев создал таблицу, в которой элементы были упорядочены по возрастанию их атомных весов. Однако он заметил закономерности в изменении химических свойств элементов в зависимости от их атомных номеров и перестроил таблицу по возрастанию атомных номеров.
Периодический закон Менделеева имеет следующую форму: элементы, расположенные в таблице по горизонтали, образуют периоды, а элементы, находящиеся в одной вертикальной колонке, образуют группы или семейства. Каждый элемент имеет свой уникальный атомный номер и химические свойства.
Периодическая система элементов является основным инструментом организации и классификации химических элементов. Она позволяет предсказывать и изучать свойства новых элементов, а также раскрывает закономерности в их химическом поведении.
Структура периодической системы основана на разделении элементов на блоки, группы и периоды. Блоки включают s-, p-, d- и f-блоки, которые характеризуют различное расположение электронных оболочек у атомов элементов. Группы образуют столбцы в таблице, а периоды — строки.
Периодическая система также позволяет предсказывать свойства элементов по их расположению в таблице. Например, элементы, находящиеся в одной группе, имеют схожие химические свойства и реактивность, так как у них одинаковое число электронов на внешней электронной оболочке.
Периодический закон Менделеева и периодическая система являются одними из основных фундаментальных принципов химии. Знание и понимание этих концепций позволяет ученым разрабатывать новые химические соединения, материалы и расширять наши знания о мире вокруг нас.
Периодический закон Менделеева
Суть периодического закона Менделеева заключается в том, что химические элементы можно упорядочить по возрастанию их атомных номеров, а при этом в периодической системе элементов можно увидеть закономерности в изменении их свойств. Вся периодическая система разделена на периоды – строки, и группы – столбцы.
В таблице Менделеева для каждого элемента указывается его атомный номер, символ и относительная атомная масса. Периодический закон позволяет предсказывать и объяснять химические свойства элементов и представляет собой удобное средство классификации элементов.
| Атомный номер | Символ | Относительная атомная масса |
|---|---|---|
| 1 | H | 1.008 |
| 2 | He | 4.0026 |
| 3 | Li | 6.94 |
| 4 | Be | 9.0122 |
| … | … | … |
Периодический закон Менделеева имеет огромное значение в химии, так как позволяет систематизировать и организовать информацию о свыше 100 известных элементах. Этот закон помогает химикам предсказывать свойства новых элементов, находить закономерности и законы, которые помогают в дальнейших исследованиях и разработке новых материалов.
История открытия и формулировка закона
Периодический закон Менделеева, также известный как периодическая система химических элементов, был открыт и сформулирован в конце XIX века русским химиком Дмитрием Менделеевым.
Менделеев заметил, что химические элементы можно упорядочить в соответствии с некоторыми закономерностями и при этом разделить их на периоды и группы.
В 1869 году Менделеев опубликовал свою периодическую систему и предсказал существование некоторых ещё неизвестных элементов. Вскоре после этого были открыты три из этих элементов: германий, галлий и скандий, что привело к ещё большей популяризации его работы.
Периодический закон Менделеева стал фундаментом химии и позволил ученым классифицировать элементы, предсказывать их свойства и выстраивать логическую структуру для изучения и понимания химических процессов.
Важно отметить, что периодический закон Менделеева был развит и изменен в дальнейшем, но его основные принципы все еще остаются основой современной периодической системы.
Основные принципы закона и их сущность
1. Периодическая закономерность
Один из основных принципов закона Менделеева заключается в том, что химические элементы следуют определенной периодической закономерности в своих свойствах. Это означает, что свойства элементов имеют тенденцию изменяться по мере их перемещения вдоль периодов и групп таблицы Менделеева. Например, ионы элементов группы 1 всегда имеют +1 заряд, а ионы элементов группы 7 всегда имеют -1 заряд.
2. Расположение элементов по атомным номерам
Закон Менделеева также основан на расположении элементов в периодической системе в порядке возрастания их атомных номеров. Атомный номер элемента определяется количеством протонов в его ядре и определяет его положение в периодической системе. Это позволяет нам легко узнавать о химических свойствах их атомов.
3. Группировка элементов по химическим свойствам
Используя закон Менделеева, элементы можно группировать по их химическим свойствам. Например, элементы группы 1 (щелочные металлы) обладают схожими химическими свойствами, такими как легкая реактивность с водой и образование гидроксидов.
4. Предсказание неизвестных элементов
Еще одной важной сущностью закона Менделеева является его способность предсказывать свойства неизвестных элементов. Менделеев оставил некоторые пропуски в своей таблице, чтобы расставить элементы в правильном порядке на основе их свойств. Этот подход позволил ему предсказывать неизвестные тогда элементы, такие как германий и галлий.
Все эти принципы закона Менделеева являются ключевыми для понимания периодической системы элементов, а также для развития химии в целом. Они позволяют ученым исследовать и классифицировать различные материалы, создавать новые соединения и предсказывать свойства новых элементов, что имеет огромное значение для наших знаний и прогресса в области химии.
Важность и применение закона в химии
Периодический закон Менделеева и периодическая система элементов имеют огромную важность в химии. Они представляют собой организацию элементов в определенном порядке, основанную на их атомных номерах и химических свойствах.
Закон Менделеева позволяет систематизировать и классифицировать все известные элементы. Он позволяет предсказывать свойства новых элементов, которые могут быть открыты в будущем. Благодаря этому закону, химики могут легко находить информацию об элементах и их свойствах, необходимую для проведения экспериментов и исследований.
Периодическая система помогает химикам легко понимать связи между элементами и их свойствами. Она позволяет предсказывать реакции между элементами и находить новые способы использования элементов. Например, периодическая таблица помогает химикам определять молекулярные формулы и реакционные уравнения.
Благодаря закону Менделеева и периодической системе элементов были открыты новые элементы, например, гелий и франций. Также они помогли предсказать свойства пустых мест в таблице элементов, что привело к открытию новых элементов — техниция, прометия, астатина и других.
Важность закона Менделеева и периодической системы элементов распространяется не только на химию, но и на многие другие области науки и технологии. Они полезны в физике, биологии, материаловедении, медицине и других дисциплинах. Эти законы также помогают развить систематический и логический подход к изучению и пониманию химических процессов.
Таким образом, закон Менделеева и периодическая система элементов играют ключевую роль в химии и науке в целом. Они обеспечивают основу для понимания свойств химических элементов, предсказания новых элементов и развития новых технологий.
Периодическая система элементов
ПСЭ создана на основе периодичности свойств химических элементов. В таблице элементы расположены по возрастанию атомного номера, а каждый горизонтальный ряд называется периодом, а каждая вертикальная группа – группой.
С помощью ПСЭ можно легко определить ключевые характеристики элементов, такие как атомный номер, атомная масса, электронная конфигурация и химические свойства. Также ПСЭ помогает установить основные тренды периодичности, такие как изменение радиуса атома, электроотрицательности и ионизационной энергии по горизонтали и вертикали таблицы.
Кроме того, систематическое расположение элементов в ПСЭ позволяет предсказать некоторые свойства еще неизвестных элементов и обнаруживать группы схожих элементов. Так, элементы одной группы обычно имеют сходные химические свойства, что делает ПСЭ полезным инструментом для химиков при изучении и предсказании реакций и взаимодействий.
Итак, ПСЭ представляет собой не только инструмент для организации и систематизации элементов, но и ключевое средство анализа и понимания химии. Она является фундаментальным элементом обучения химии и способствует развитию новых технологий и научных исследований.
Основные принципы построения и структура системы
Первый принцип – периодичность химических свойств. Менделеев открыл, что вещества обладают сходными свойствами, если их атомные массы находятся в одной периодической закономерности. Это позволяет расположить элементы в порядке возрастания атомных масс таким образом, чтобы элементы с похожими химическими свойствами находились на одной горизонтали.
Второй принцип – периодическое возрастание атомных масс. Элементы Периодической системы расположены таким образом, что атомные массы возрастают с левого верхнего угла к правому нижнему углу. Это приводит к постепенному изменению свойств элементов вдоль периодов.
Третий принцип – группировка элементов схожими свойствами. Вертикальные столбцы в Периодической системе называются группами или семействами элементов. Элементы в одной группе имеют схожие химические свойства, так как у них одинаковое число электронных оболочек или одинаковое число валентных электронов. Это позволяет легко предсказывать свойства новых элементов и сравнивать их с уже известными.
Четвёртый принцип – предсказуемость свойств элементов. С помощью Периодической системы можно установить связь между строением атома и его химическими свойствами. Менделеев использовал эту связь для предсказания свойств ещё неизвестных элементов и даже указал на их примерные атомные массы и химические свойства. Предсказания Менделеева были впоследствии подтверждены открытием новых элементов.
Используя основные принципы построения и структуры Периодической системы, ученые смогли классифицировать и систематизировать свыше 100 элементов. Эта система продолжает быть жизненно важным инструментом для понимания свойств и поведения химических элементов.
Вопрос-ответ:
Каково значение периодического закона Менделеева в химии?
Периодический закон Менделеева является одним из основных законов химии. Он позволяет систематизировать и классифицировать химические элементы, а также предсказывать их свойства и поведение в различных химических реакциях. Периодический закон основан на упорядочении элементов по возрастанию атомного номера и расположении их в виде таблицы, известной как периодическая система элементов.
Какие элементы включает периодическая система Менделеева?
Периодическая система Менделеева включает в себя все известные химические элементы. На данный момент она состоит из 118 элементов, начиная с самого легкого — водорода (H) и заканчивая самым тяжелым — оганессоном (Og). Элементы в периодической системе расположены в порядке возрастания атомного номера и разделены на блоки, группы и периоды в соответствии с их электронной конфигурацией и химическими свойствами.
Какова структура периодической системы элементов?
Периодическая система элементов имеет следующую структуру. Она состоит из семи горизонтальных строк, называемых периодами, и 18 вертикальных столбцов, называемых группами. В каждом периоде количество элементов увеличивается от одного в первом периоде до 32 (включая искусственные элементы) в седьмом периоде. Группы элементов имеют общую химическую природу и схожие химические свойства. Отдельные блоки в периодической системе также отражают особенности электронной конфигурации элементов и их благоприятность для различных типов химических реакций.
Какие пользу извлекает химия от периодического закона Менделеева?
Периодический закон Менделеева является важным инструментом в химии, который приносит множество пользы. Он помогает ученым систематизировать и классифицировать элементы, что позволяет разрабатывать новые материалы и соединения, исследовать и предсказывать их свойства и поведение в химических реакциях. Периодический закон также позволяет легко находить информацию о различных элементах, их атомных номерах, массовых долях, электронной конфигурации и других характеристиках. Это особенно полезно при проведении экспериментов и при изучении различных аспектов химии.
Каково значение периодического закона Менделеева в химии?
Периодический закон Менделеева является основополагающим принципом для организации и классификации элементов, который широко используется в химии. Он позволяет предсказывать свойства элементов, определять их электронную структуру и реакционную способность, а также строить периодическую систему элементов.